R&Dグレード mRNA製造受託
in vitro転写によるmRNA製造ワークフロー
mRNAは多様な疾患に対する革新的な治療手段として注目されています。当社のmRNA合成サービスは、鋳型プラスミドの設計・構築からIVTによるmRNA合成まで、独自のプラットフォームで一貫して最適化しています。
-

mRNA設計支援
-

人工遺伝子合成
-

mRNA合成
条件検討 -

mRNA合成
本製造 -

LNP化
ニーズに応えるオーダーメイドなmRNA合成
当社のサービスは、お客様のプロジェクト要件に合わせて柔軟にカスタマイズ可能です。創薬初期段階でmRNAを設計・最適化することで、後工程のスケールアップやGMP製造へのシームレスな移行をより確実にします。

| 5’Cap | ORF | 修飾核酸 | UTR | Poly A |
|---|---|---|---|---|
| ・CleanCap ® M6 ・CleanCap ® AG ・CleanCap ® AG 3’OMe ・Enzymatic capping ・Uncapped |
・Catalog sequence ・Customer’s sequence ・Codon optimization ・Linker strategies |
・N1-Methyl-Pseudo-UTP ・5-Methoxy-UTP ・Pseudo-UTP ・5-Methyl-UTP ・5-Methyl-CTP ・Unmodified |
・Our standard UTRs ・Customer’s UTRs ・UTR optimization |
・120 nt A tail ・100 nt A tail ・80 nt A tail ・Custom tail length ・Linker strategies |
*当社は、TriLink Biotechnologies, Inc.(以下「Trilink社」)より、革新的な5’キャップ付加技術「CleanCap®」のライセンスを受けております。
その他オプション
| 精製 | LNP化 |
|---|---|
| ・シリカカラム+遠心精製 ・Oligo dT法 ・逆相LC法 ・その他(ご相談) |
・標準推奨処方 ・お客様処方 |
各種最適化オプション

キャッピング
mRNA分子の5′末端にキャップ構造を付与することで、エキソヌクレアーゼによる分解耐性が大幅に向上し、細胞内での安定性と翻訳効率が飛躍的に高まります。Enzymatic法は柔軟性が高く、CleanCap®は高純度かつ一段階で高キャッピング率を実現します。
修飾核酸
ウリジンなどの塩基を化学修飾することで、パターン認識受容体(TLRなど)による免疫誘導を抑制し、炎症反応を最小化します。特にUTP修飾は翻訳効率を損なわずに免疫原性を低減し、タンパク質発現の持続性を向上させます。
修飾核酸導入による分解耐性向上
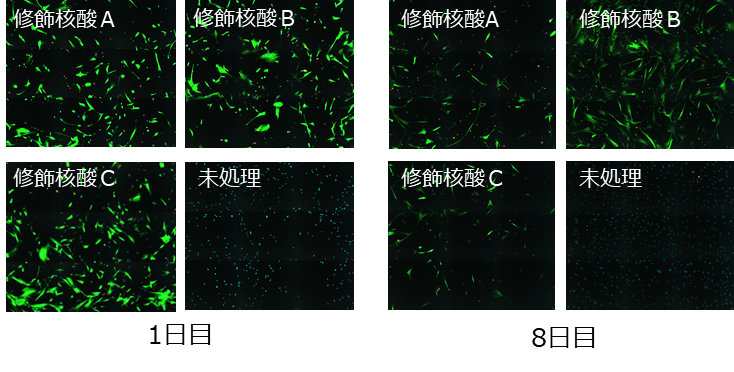
ヒト繊維芽細胞において、修飾核酸Aを用いた合成GFP mRNAでは、8日後においても強いGFP蛍光が観察されました。

UTR最適化
5′-および3′非翻訳領域(UTR)の配列や二次構造を最適化することで、リボソームの結合と再利用効率が改善し、mRNAの安定性および翻訳持続時間を延長します。安定化シグナルやRNA結合タンパク質の認識サイトを適切に配置することがポイントです。
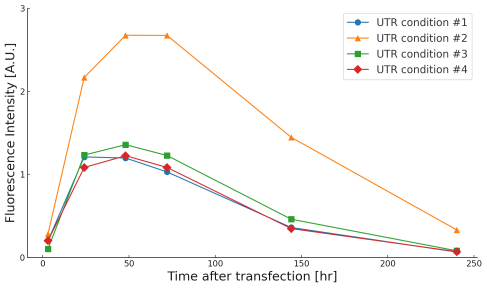
Cell: HEK293
CDS: eGFP
Cap: CleanCap® Reagent AG (3’OMe)
Modified nucleic acid: N1-Methyl-ΨU

コドン最適化
目的タンパク質のアミノ酸配列を変えずに、発現宿主細胞で利用頻度の高いコドンへ置き換えることで、リボソームの翻訳速度が向上し、タンパク質産生量を最大化します。GC含量や二次構造も考慮し、翻訳効率とmRNA安定性を両立させます。
精製
不完全転写産物やダイマー、DNA鋳型残渣などの不純物を徹底的に除去することで、誘導される免疫反応や細胞毒性を低減し、安全性および再現性を確保します。Oligo-dT法や逆相LC法など、用途に応じた精製プロセスを選択します。

LNP化
脂質ナノ粒子(LNP)に封入することで、mRNAを血中や組織間の分解酵素から保護し、標的細胞への取り込み効率を飛躍的に向上させます。LNPは内在化後のエンドソーム脱出を促進し、細胞質内でのmRNA放出を最適化します。
提供形態
お客様のアプリケーションニーズに合わせて、必要なフォーマットと量のmRNAをスムーズにご提供します。

Discovery Package : 初期スクリーニング目的での少量多品種製造
| 納品量 | 100 μg(保証収量: 50 μg※1) |
|---|---|
| Capping | CleanCap AG₋3’OMeを推奨※1 |
| 修飾核酸 | N1-Methyl-Pseudo-UTPを推奨※1 |
| 鋳型 | お客様よりご提供 または 鋳型合成費用込みのパッケージ |
| 品質確認 | 濃度試験(NanoDrop)/ 完全性試験(CE) |
| 価格 | IVTのみ 100,000円 / 鋳型合成+IVT 200,000円 |

Research Package : Vitro/Vivo実験目的でのNon-GMP製造
| 納品量 | 0.5~100 mg(保証収量:目標の50%) |
|---|---|
| Capping | CleanCap または Enzymatifc Capping※1 |
| 修飾核酸 | UTPの各種修飾を推奨※1 |
| 鋳型 | 鋳型合成費用込みのパッケージ |
| 品質確認 | 濃度試験(NanoDrop)/ 完全性試験(CE)/ エンドトキシン等 |
| 価格 | お問合せ |

Preclinical Package : Tox目的でのNon-GMP製造
| 納品量 | 100~1000 mg(保証収量:目標の80%) |
|---|---|
| Capping | CleanCap、またはEnzymatifc Capping※1 |
| 修飾核酸 | UTPの各種修飾を推奨(ご相談可能) |
| 鋳型 | 鋳型合成費用込みのパッケージ |
| 品質確認 | 試験項目はUSP3.0*に準拠※1, 2 |
| 価格 | お問合せ |
※1 ご相談可能
※2 2025年5月時点
品質管理
mRNAの品質試験を提供します。mRNA医薬特有の分析項目は国内設備を利用するため、迅速かつ柔軟な対応が可能です。
(mRNA合成の追加オプションとしてお受けします。)
| Quality | Attribute | Method | Discovery Pack |
リサーチ | 前臨床 | |
|---|---|---|---|---|---|---|
| Identity | 配列確認 | サンガーシーケンス | - | - | 対応 | |
| Content | RNA 含量測定 (濃度・A260/A280 ratio) |
吸光度 (UV) | 対応 | 対応 | 対応 | |
| Integrity | mRNA 完全性 | キャピラリーゲル電気泳動(CGE) | 対応 | 対応 | 対応 | |
| Purity | 純度確認 | 要相談 | - | - | - | |
| 5’ キャップ化効率 | LC-MS | - | 対応 | 対応 | ||
| 3’ poly(A) tail 長 | LC-MS | - | - | 対応 | ||
| Product 由来の不純物 | dsRNA | ELISA | - | 対応 | 対応 | |
| 凝集率 | 要相談 | - | - | - | ||
| 短鎖混入率 | 要相談 | - | - | - | ||
| 残存 DNA Template | qPCR | - | - | 対応 | ||
| 残存ヌクレオチド | 要相談 | - | - | - | ||
| 残存試薬等 | 要相談 | - | - | - | ||
| 残存 T7 polymerase | ELISA | - | - | 対応 | ||
| Potency | タンパク発現 | 要相談 | - | - | - | |
| Safety | エンドトキシン試験 | USP <85>、JP<4.01> | - | 対応 | 対応 | |
| 微生物限度試験 | USP <61>, <62>, <1115> JP<4.05> |
- | - | 対応 | ||
| Other | 性状確認 | USP <790> | 対応 | 対応 | 対応 | |
| 残存溶媒 | USP <467>、JP<2.46> | - | - | 対応 | ||
| pH | USP <791>、JP<2.54> | - | - | 対応 | ||
Ref. : Analytical Procedures for Quality of mRNA Vaccines and Therapeutics (Draft Guidelines: 3rd Edition)
※追加の品質管理および評価をご希望の場合は、お問い合わせください。